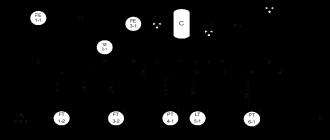
На рис. приведена диаграмма состояния Al—Mg. Средняя часть диаграммы показана в увеличенном масштабе.
В системе образуются фазы β(Al3Mg2), γ(Al12Mgl7), ζ(Al52Mg48), ε(Al30Mg23). Фазы β и γ плавятся конгруэнтно при температурах 453 и 460 °С, соответственно. Фазы ε и ζ образуются по перитектическим реакциям при температурах 450 и 452 °С, соответственно.
В системе существуют три эвтектических равновесия: Ж ↔Mg+ γ при температуре 438 °С, Ж ↔(А1) + β при 450 °С, Ж ↔ε + β при 448 °С, а также два эвтектоидных равновесия ε↔ β + ζ при -428 °Cи ζ ↔β + γ при 410 °С.
Растворимость Mgв (А1) исследована во многих работах.
Растворимость Mg:
% (ат.) ......................
% (по массе) .............
Максимальная растворимость Mgв (А1) определена равной 16,5 % (ат.), так же как и в ряде других работ, где не был использован метод рентгеновского анализа. Данные по растворимости А1 в (Mg), полученные в разных исследованиях, также различаются. Наиболее вероятны значения, приведенные ниже:
Растворимость Аl:
% (ат.) .....................
% (по массе) ............

Источники:
- Диаграммы состояния двойных и многокомпонентных систем на основе железа. Банных О. А., Будберг П.Б., Алисова С. П. и др. Металлургия, 1986 г.
- Двойные и многокомпонентные системы на основе меди. под ред. Шухардина С.В. Наука, 1979 г.
- Диаграммы состояния двойных металлических систем ред. Лякишева Н.П.Машиностроение, 1996-2000 г.
К сплавам системы Al-Mg относится большая группа широко используемых в промышленности сплавов: АМг0,5; ; ; ; ; ; . Из них изготавливают почти все виды полуфабрикатов: листы, плиты, поковки, штамповки, прессованные изделия (прутки, профили, панели, трубы) и проволоку. Все сплавы рассматриваемой группы хорошо свариваются всеми видами сварки.
Полуфабрикаты из этих сплавов имеют относительно высокий уровень прочностных характеристик по сравнению с другими термически неупрочняемыми сплавами. Так, минимальные значения предела текучести для листового материала (толщина ~2 мм) в отожженном состоянии для указанного ряда сплавов соответственно равны 30, 40, 80, 100, 120,150 и 160 МПа. Временное сопротивление, как правило, в два раза выше предела текучести, что свидетельствует об относительно высокой пластичности этих сплавов. Однако они довольно быстро нагартовываются, что отрицательно влияет на их технологическую пластичность. Последняя значительно понижается с увеличением концентрации магния. Поэтому сплавы с содержанием магния более 4,5 % можно отнести к «полутвердым» и даже «твердым» сплавам.
Отрицательная роль повышенного содержания магния в большей степени проявляется при изготовлении прессованных изделий. Сплавы с высоким содержанием магния прессуются с низкими скоростями (в десятки раз меньшими, чем, например, некоторые сплавы системы Al-Zn-Mg или Al-Mg-Si), что существенно понижает производительность прессовых цехов. Производство катаных полуфабрикатов из сплава АМг6 - процесс трудоемкий. Поэтому в последнее время высоколегированные магналии стали заменять более технологичными сплавами, например, сплавами на основе системы Al-Zn-Mg (1935, 1915, 1911), которые значительно превосходят сплав АМг6 по прочностным свойствам (особенно по пределу текучести) и не уступают ему по многим коррозионным характеристикам.
Низколегированные магналии с содержанием магния до 3 % найдут еще более широкое применение вследствие их высокой коррозионой стойкости и пластичности. Согласно диаграмме состояния сплавов Al-Mg, при температуре эвтектики в алюминии растворяется 17,4 % Mg. При понижении температуры эта растворимость резко снижается и в области комнатных температур составляет примерно 1,4 %.
Таким образом, сплавы с большим содержанием магния в обычных условиях имеют пересыщение по этому элементу (зависящее от марки сплава), и, следовательно, в них должен проявляться эффект старения. Однако структурные изменения, протекающие в этих сплавах в процессе распада твердого раствора, практически не оказывают никакого влияния на уровень прочностных характеристик и в то же время резко изменяют коррозионную стойкость полуфабрикатов. Причина такого аномального поведения заключается в характере распада твердого раствора и фазовом составе выделений. Поскольку для сплавов Al-Mg верхняя температурная граница образования зон ГП (или критическая температура растворимости зон ГП - t K) значительно ниже комнатной температуры, то распад твердого раствора происходит по гетерогенному механизму с образованием переходной (В`) и равновесной (В-Mg 2 Al3) фаз. Эти выделения зарождаются гетерогенно на границах раздела (зерна, интерметаллидные частицы и т. п.), а также дислокациях и поэтому их вклад в процесс упрочнения невелик и полностью компенсируется степенью разупрочнения, обусловленного снижением концентрации магния в твердом растворе. По этой причине на практике и не наблюдается эффекта упрочнения сплавов этой группы при распаде твердого раствора в процессе естественного или искусственного старения пли при различных режимах отжига.

Фаза В в нейтральном водном растворе хлоридов (3 % NaCl) имеет отрицательный потенциал коррозии, равный - 0,930 В. В этом же растворе, но при меньших значениях рН, т. е. в кислой среде, разница потенциалов между фазой и твердым раствором хотя и уменьшается, но остается достаточно большой: (-0,864 В) - - (-0,526 В) =0,338 В. И, наоборот, в щелочной среде (3% NaCl+1% NaOH) алюминий и сплавы алюминия, содержащие 1- 9 % Mg, становятся отрицательнее В-фазы, и разница потенциалов для крайних значений указанной области концентрации магния соответственно составляет +0,24 и +0,18 В. Рассмотренные особенности изменения электрохимических характеристик отдельных структурных составляющих сплавов А1-Mg в зависимости от внешней среды в основном и определяют сопротивление этих сплавов МКК, РСК и КР.
Из изложенного следует, что сплавы с содержанием магния более 1,4% потенциально могут быть чувствительны к одному, двум или всем указанным ранее видам коррозии. Однако большой опыт эксплуатации конструкций и многочисленные эксперименты показывают, что практически сплавы с концентрацией магния, не превышающей 3,5% (AMrl, АМг2 и частично АМг3), не проявляют чувствительности к КР и РСК (рис. 56).
Электронно-микроскопические исследования показывают, что это связано с дискретным распределением частиц В-фазы по границам зерен в связи с малым пересыщением твердого раствора. Поэтому процесс коррозии в нейтральных и кислых средах ограничивается лишь только электрохимическим растворением тех частиц, которые выходят на поверхность сплава, непосредственно контактирующего с электролитом.
Такие сплавы коррозионно устойчивы и в нагартованном состоянии, т. е. хотя нагартовка и ускоряет распад твердого раствора, однако она не изменяет характера распределения выделений на границах зерен. В то же время за счет благоприятного в этом случае влияния структурной анизотропии сопротивление коррозионному питтингу существенно возрастает. Сплавы с содержанием магния более 3,5 % (АМг3, АМг4) и особенно более 5 % (АМг5, АМг6) в определенном структурном состоянии и при определенных условиях внешней среды могут быть чувствительны к МКК и РСК, а также и к КР.
Для сплавов системы Al-Mg электрохимические факторы в коррозионном растрескивании играют значительно большую роль, чем для сплавов других систем. Поэтому предотвращение образования пленки В-фазы по границам зерен целесообразно и для повышения сопротивления КР. В производственных условиях именно такой способ повышения сопротивления КР среднелегированных магналиев нашел широкое распространение.
Для малолегированных сплавов с содержанием магния более 1,4 % использование методов термической и термомеханической обработки, способствующих равномерному распределению В-фазы играет меньшую роль, чем для средне- и высоколегированных. Однако в полунагартованном состоянии, полученном с использованием эффекта НТМО, кроме появления структурной анизотропии, тормозящей распространение коррозии вглубь, положительное влияние оказывает, по-видимому, также более равномерное распределение В-фазы. Например, глубина коррозии на листах из сплава АМг2, подвергнутых ТМО, значительно уменьшается по сравнению с глубиной коррозии на обычных нагартованных листах.
Рост глубины локальных поражений у сплава АМг2 в отожженном состоянии в условиях морской атмосферы можно также частично связать с неоднородностью выделений В-фазы. Таким образом, для сплава АМг2 целесообразно использовать технологию, позволяющую получать равномерное распределение избыточной фазы. Однако и при использовании обычной технологии малое содержание легирующих элементов оказывается решающим фактором в определении коррозионной стойкости этого сплава. Подтверждением этому служит достаточно высокая коррозионная стойкость сплава АМг2 в разных средах.
Характерным примером является поведение магналиев в морской воде. Сплав типа АМг2 после 10 лет испытаний имел коррозионную стойкость, весьма близкую к той, которую он имеет в морской атмосфере (табл. 30).

Сплав типа АМг4 имеет значительно большую глубину коррозионного питтинга в морской воде, чем сплав типа АМг2. Для сплава типа АМг5 максимальная глубина питтинга возрастает еще более резко.
Таким образом, в морской воде существует четкая корреляция между чувствительностью к структурной коррозии (т. е. коррозионному растрескиванию и расслаивающей коррозии) и обычным питтингом. С ростом степени легированности возрастает пересыщение твердого раствора и соответственно чувствительность к структурной коррозии, связанная с тенденцией к избирательному выделению В-фазы. В этой связи для сплавов АМг4, АМг5 и особенно АМг6 возрастает роль технологических факторов, обусловливающих равномерное распределение В-фазы в сплаве.
Одним из эффективных способов повышения коррозионной стойкости среднелегированных магналиев является ТМО. В соответствии с этим максимальное сопротивление РСК и КР может быть достигнуто лишь при формировании в полуфабрикатах полигонизованной структуры в сочетании с равномерным распределением второй фазы. Положительных результатов можно добиться, используя также на окончательной стадии обработки режимы отжигов с температурой ниже линии растворимости магния в алюминии. При этом следует учитывать, что полуфабрикаты с разной степенью рекристаллизации ведут себя по-разному. В настоящее время конструкции изготавливают из отожженных полуфабрикатов с частично (прессованные и горячекатаные полуфабрикаты) и полностью рекристаллизованной (холоднокатаные листы и трубы) структурой. Поскольку в зависимости от характера структуры изменяются корреляционные связи между технологическими параметрами и коррозионными свойствами, рассмотрим влияние отжига раздельно для холодно- и горячедеформированных полуфабрикатов.
Лектор В.С.ЗолоторевскийОбщие сведенияОбласти применения
Первичный алюминий
Роль примесей и легирующих элементов
Основные системы легирования и классификация
сплавов
Cтруктура и свойства слитков и отливок
Структура и свойства деформированных
полуфабрикатов
Промышленные алюминиевые сплавы
(доклады студентов)
09.02.2017
2
Учебная литература
И.И. Новиков, В.С. Золоторевский, В.К. Портной идр. Металловедение, том 2. МИСиС, 2014. (Глава 15)
Б.А. Колачев, В.И. Ливанов, В.И. Елагин.
Металловедение и термическая обработка цветных
металлов и сплавов. МИСиС, 2005.
В.С. Золоторевский, Н.А. Белов. Металловедение
цветных металлов. Раздел: Алюминиевые сплавы.
МИСиС, 2000. (№ 1564).
Другая литература (не менее 5 источников)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
3
Темы докладов c презентацией
1.2.
3.
4.
5.
6.
Силумины
Дуралюмины
Магналии
Жаропрочные алюминиевые сплавы
Высокопрочные алюминиевые сплавы
Литийсодержащие алюминиевые сплавы
В докладах (20-30 минут) рассматриваются химический состав,
структура и свойства промышленных сплавов, области
применения
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
4
Общая характеристика алюминия и его сплавов
Большие запасы (8%Al) в земной коре1-е место среди цветных металлов по объему
производства – более 30 млн т/год (15% РФ)
Цена - 1500-2600 $/т (~1500 $/т)
Легкость – уд.вес 2,7 г/см3
Высокая прочность (сплавов)- в до 700 МПа
Высокая коррозионная стойкость
Высокая электропроводность (2/3 от Cu)
Высокая технологичность при всех видах обработки
Возможность использования отходов
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
5
Области применения алюминия и его сплавов
авиа- и ракетостроениеназемный и водный транспорт
машиностроение
электротехника
строительство
упаковка (для пищи, лекарств и т.д.)
бытовая техника
специальные области
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
6
ПЕРВИЧНЫЙ АЛЮМИНИЙ Химический состав некоторых стандартных марок первичного алюминия (ГОСТ 11069-2001) «Вторичный алюминий» - Al-сплавы из лома
ПЕРВИЧНЫЙ АЛЮМИНИЙХимический состав некоторых стандартных марок первичного
алюминия (ГОСТ 11069-2001)
«Вторичный алюминий» - Al-сплавы из лома и отходов
Марка
Fe, %
Si, %
Cu, %
Zn, %
Ti, %
Ост., %
Всего
примесей, %
Al, %
не
менее
высокой чистоты
А995
0,0015
0,0015
0,001
0,001
0,001
0,001
0,005
99,995
А99
0,003
0,003
0,002
0,003
0,002
0,001
0,01
99.99
А97
0,015
0,015
0,005
0,003
0,002
0,002
0,03
99,97
А95
0,03
0,03
0,015
0,005
0,002
0,005
0,05
99,95
технической чистоты
А85
0,08
0,06
0,01
0,02
0,01
0,02
0,15
99,85
А7
0,16
0,15
0,01
0,04
0,02
0,02
0,30
99,70
А5
0,30
0,25
0,02
0,06
0,03
0,03
0,30
99,50
A35
0,65 (Fe+Si)
0,05
0,1
0,02
0,03
1,00
99,35
A0
0.95 (Fe+Si)
0,05
0,1
0,02
0,03
1,00
99,00
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
7
Физические свойства Al в сравнении с другими металлами
СвойствоAl
Fe
Cu
Температура плавления, 0С
660
1539
1083
650
1652
Температура кипения, 0С 2494
Плотность, г/см3
2872
2,7
2595
7,86
1107
8,9
3000
1,738
4,5
Коэфф. терм. расш., 106* К-1
23,5
12,1
17,0
26,0
8,9
Уд. электросопр., 108* Ом*м
2,67
10,1
1,69
4,2
54
Теплопроводность, Вт*м-1*К-1
238
78,2
397
156
21,6
Теплота плавления, Дж*г-1
405
272
205
293
358
Теплота испарения, кДж*г-1
10,8
6,1
6,3
5,7
9,0
Модуль упругости, ГПа
70
220
132
44
112
Mg
Ti
У чистого Al низкая твердость - 10-15НВ, прочность в=50-70 МПа и высокая
пластичность =30-45%
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
8
Основные примеси в алюминии и его сплавах
ЖелезоКремний
Fe+Si – фазы Al3Fe, Al5FeSi (β) и Al8Fe2Si (α)
Цинк
Медь
Магний
Свинец и олово
Натрий
Водород
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
9
10. ОСНОВНЫЕ БАЗОВЫЕ СИСТЕМЫ ЛЕГИРОВАНИЯ ПРОМЫШЛЕННЫХ АЛЮМИНИЕВЫХ СПЛАВОВ
Al-Si, Al-Si-Mg (силумины)Al-Si-Cu-Mg (медистые силумины)
Al-Cu [-Mn] (жаропрочные)
Al-Mg (магналии)
Al-Mg-Si (авиали)
Al-Cu-Mg (дуралюмины)
Al-Cu-Mg-Si (ковочные)
Al-Zn-Mg (свариваемые)
Al-Zn-Mg-Cu (высокопрочные)
Al-Li-Cu-Mg (сверхлегкие)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
10
11. Классификация легирующих элементов и примесей в промышленных алюминиевых сплавах по их влиянию на образование различных элементов струк
Классификация легирующих элементов и примесей впромышленных алюминиевых сплавах по их влиянию на
образование различных элементов структуры
Элементы структуры,
образуемые добавками и
примесями
Легирующие
элементы и примеси
Твердый раствор (Al) и основные фазы Cu, Mg, Si, Zn, Li, (Mn) –
-упрочнители при старении
основные легирующие
элементы - сл.12-14
Нерастворимые (при отжиге) эвтекти- Fe, Si, Ni, Mn, (Mg, Cu)
ческие фазы
Первичные кристаллы
Fe, Ni, Mn, Si, (Zr, Cr, Ti)
Дисперсоиды при высокотемператур- Mn, Zr, Cr, Ti, Sc (иногда
ных нагревах
+Сu, Fe, Si и др.)
Микродобавки, мало влияющие на Be, Cd, Sr, Na, Ti, B
09.02.2017
фазовый состав Курс “Структура и свойства цветных металлов и сплавов“
11
12. Диаграмма состояния Al-Cu
13. Диаграмма состояния Al-Mg
14. Диаграмма состояния Al-Si
15. Характеристики диаграмм состояния эвтектического типа, образуемых алюминием с основными легирующими элементами
№Легирую- Сп,
щие
мас.%
элементы (ат.%)
Се,
мас.%
(ат.%)
Tпл,
0C
Фаза в равновесии с (Аl)
(содержание
второго
компонента, мас.%)
1
Cu
5,7 (2,5)
33,2
(17,5)
548
CuAl2 (52%Cu)
2
Mg
17,4 (18,5) 35
(36) 450
Mg5Al8 (35%Mg)
3
Zn
82
(49,3)
94,9
(75) 382
(Zn)
(>99%Zn)
4
Si
1,65
(1,59)
12
(12)
(Si)
(>99,5%Si)
09.02.2017
577
Курс “Структура и свойства цветных металлов и сплавов“
15
16. Характеристики двойных фазовых диаграмм алюминия с переходными металлами, присутствующими в алюминиевых сплавах в качестве примесей или
Характеристики двойных фазовых диаграмм алюминия спереходными металлами, присутствующими в алюминиевых
сплавах в качестве примесей или легирующих элементов (см. слайд
11)
№
Легирующие
элементы
(тип диаграммы)
Сп,
масс.%
(ат.%)
1
Fe (e)
0,05
(0,03) 1,8
(0,9) 655
FeAl3 (40%Fe)
2
Ni (e)
0,04
(0,02) 6,0
(2,8) 640
NiAl3 (42%Ni)
3
Ce (e)
0,05
(0,01) 12
(2,6) 650
CeAl4 (57%Ce)
3
Mn (e)
1,8
(0,89) 1,9
(0,91) 658
4
Sc (e)
0,3
(0,2)
0,6
(0,4) 655
ScAl3 (36%Sc)
5
Ti (p)
1,3
(0,8)
0,12
(0,08) 661
TiAl3 (37%Ti)
6
Zr (p)
0,28
(0,1)
0,11
(0,04)
661
ZrAl3 (53%Zr)
7
Cr (p)
0,8
(0,4)
0,4
(0,2) 661
CrAl7 (22%Cr)
09.02.2017
Се,p ,
мас.%
(ат.%)
Te,p, 0C
Фаза в равновесии с
(Аl)
(содержание
второго компонента,
масс.%)
MnAl6 (25%Mn)
Курс “Структура и свойства цветных металлов и сплавов“
16
17. Области составов алюминиевых сплавов и их классификация по структуре
1.Сплавы типа твердых растворов(матричные) (подавляющее
большинство деформируемых
сплавов, а также литейные на
базе систем Al–Cu, Al–Mg и AlZn-Mg);
2.Доэвтектические сплавы
(большинство силуминов сплавов, в которых важнейшим
легирующим элементом является
кремний, например типа АК7 и
АК8М3, а также некоторые
деформируемые сплавы, в
частности типа АК4-1);
3.Эвтектические сплавы (силумины
типа АК12 и АК12М2);
4.Заэвтектические сплавы
(заэвтектические силумины,
например АК18).
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
17
18.
Общие особенностиструктуры и свойств слитков
и отливок из алюминиевых
сплавов
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
18
19. Неравновесная кристаллизация
Микроструктурасплава Al-5% Cu
Н
е
09.02.2017
Неравновесная кристаллизация – результат
неполного прохождения диффузии при
реальных скоростях охлаждения
Курс “Структура и свойства цветных металлов и сплавов“
19
20. Метастабильные варианты фазовых диаграмм Al-ПМ
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
20
21. Типичная макро- и микроструктура доэвтектических литых алюминиевых сплавов
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
21
22. Микроструктуры литых сплавов
23. ХАРАКТЕРИСТИКИ ЛИТОЙ СТРУКТУРЫ
1) форма и размер кристаллитов (зерен) ;2) форма и размер дендритных ячеек (Al);
3) состав, структура, морфология и объемная доля частиц
избыточных фаз кристаллизационного происхождения
4) распределение легирующих элементов и примесей в
(Al)
5) характеристики субструктуры (распределение и
плотность
дислокаций,
размеры
субзерен
и
дислокационных ячеек, углы их разориентировки,
вторичные выделения);
6) количество, размер и распределение пор
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
23
24. Соотношение между размером дендритной ячейки (d) и скоростью охлаждения (Vохл) d=A V-nохл
Vохл, K/c10-3
d, мкм
1000
Условия получения отливок
100
100
Непрерывное
литье
103
10
Литье крупных гранул (в воду)
106
1
Получение чешуек (спиннингование)
109
0,1
Получение ультратонких чешуек
09.02.2017
Литье крупных отливок в землю
литье
слитков,
Курс “Структура и свойства цветных металлов и сплавов“
кокильное
24
25. Концентрационная граница появления неравновесной эвтектики (Ск на cлайде 20)
Концентрационная граница появлениянеравновесной эвтектики (С на cлайде 20)
к
С, %
Cu
Mg
Zn
Si
Равновесная
предельная
растворимость
Сп, %
5,65
17,4
82,2
1,65
0,5-2 K/мин
0,1
4,5
20,0
0,1
80-100 K/мин
0,1
0,5
2,0
0,1
1000 K/мин
0,3
1,0
3,0
0,2
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
25
26. Объемная доля (QV) и размер (m) частиц избыточных фаз и пор
QV = Cx/Ce)1/(1-К),где
Сe – эвтектическая концентрация,
К - коэффициент распределения (Сж/Cтв),
Сx - концентрация легирующего элемента в сплаве.
m = Bd,
где d – размер дендритной ячейки
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
26
27. МОРФОЛОГИЯ ИЗБЫТОЧНЫХ ФАЗ
Большое количество и разнообразие формы частиц избыточных фаз, втом числе одной и той же фазы при кристаллизации в разных
условиях:
1) прожилки по границам дендритных ячеек;
2) скелеты;
3) иглы, пластины;
4) тонкодифференцированные кристаллы (внутри
эвтектики) в сплавах, близких к эвтектической точке и др.
С увеличением скорости охлаждения и кристаллизации размеры частиц
уменьшаются
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
27
28. Разная морфология избыточных фаз
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
28
29. Модифицирование литой структуры
Модифирование для измельченияпервичных кристаллов
Примеры модификаторов: зерна (Al) - Ti и
Ti+B, первичного (Si) – Cu+P
Модифицирование эвтектик
Модификаторы (Si) в эвтектике: хлориды, Sr,
РЗМ – изменяют форму монокристаллов,
кристаллизующихся внутри эвтектических
колоний
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
29
30. Основные Fe- и Si-содержащие фазы в алюминиевых сплавах
Al3Fe, α(Al8Fe2Si), β(Al5FeSi)Al15(Fe,Mn)3Si2
Al6(Fe,Cu,Mn), Al7FeCu2
Al9FeNi
Al8FeMg3Si6
Распределение легирующих элементов по сечению
дендритных ячеек (Al) - слайд 23
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
30
31. Внутренняя структура дендритов (Al)
32.
Изменение структуры исвойств слитков и отливок
при гомогенизационном
отжиге
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
32
33. Структурные изменения при гомогенизации и закалке
растворение неравновесного избытка фазкристаллизационного происхождения;
2) устранение внутрикристаллитной ликвации
легирующих элементов;
3) распад алюминиевого раствора во время
изотермической выдержки с образованием
алюминидов переходных металлов (в сплавах,
содержащих такие добавки);
4)
изменение
морфологии
фаз
кристаллизационного
происхождения,
не
растворимых в твердом растворе
1)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
33
34. Растворение неравновесных фаз в результате диффузии
гдеP= (Q ·A·d/2) / (D·S·(B+K·Q) ,
P - время полного растворения -фазы
d - размер дендритной ячейки;
Q - объемная доля неравновесной -фазы;
S - суммарная поверхность ее включений;
D - коэффициент диффузии легирующего элемента в
(Al);
A, В и К - коэффициенты, постоянные для сплава
заданного состава
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
34
35. Растворение неравновесных фаз
Эмпирические уравнения:p=b0 + b1m или p = amв,
где m – толщина растворяющихся частиц
- отливки сплава АМг9 при температуре
гомогенизации 4400С p = -1,6 + 0,48m,
- слитки сплава Д16 при температуре гомогенизации
4800C р = 0,79 + 1,66m или
p = 0,63 m1,2 (m - в мкм, p - в час).
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
35
36. Устранение внутрикристаллитной ликвации
= 5,8l02/(2D),где l0 = d/2
D- коэф. диффузии при Тгом, см2/c:
Mg, Zn, Si - 10-9
Cu - 10-10
Ni - 10-12
Fe, Mn, Cr, Zr -10-13 - 10-14
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
36
37. Дисперсоиды алюминидов Mn, Zr и Ti
38. Фрагментация и сфероидизация эвтектического кремния при нагреве под закалку
39.
Структурные изменения пригомогенизации и закалке
(продолжение слайда 33)
5) изменение зеренной и дислокационной
структуры алюминиевого твердого раствора;
6) распад алюминиевого раствора по основным
легирующим элементам при охлаждении после
изотермической выдержки;
7) развитие вторичной пористости.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
39
40. Тонкая структура после закалки и старения отливок (ПЭМ)
41.
Общие особенностиструктуры и свойств
деформированных
полуфабрикатов
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
41
42. . СТРУКТУРА И СВОЙСТВА ДЕФОРМИРОВАННЫХ ПОЛУФАБРИКАТОВ ИЗ АЛЮМИНИЕВЫХ СПЛАВОВ
Деформация:«холодная» - при комнатной температуре
теплая - между комнатной и
0,5-0,6 Тпл
горячая- выше 0,5-0,6 Тпл
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
42
43. Напряжение течения
Напряжение течения-
холодной и теплой деформации алюминия напряжение течения непрерывно
растет с момента начала деформации и вплоть до разрушения по степенному
закону:
- При
где и m - коэффициенты, m < 1
- При горячей ОМД
= m,
σ примерно постоянно (установившаяся стадия)
после 10-50%-ной деформации
- Совместное влияние температуры Т и скорости деформации на σ
определяется (через структуру) параметром Зинера-Холомона:
Z = exp(Q/kTдеф).
σ линейно зависит от lgZ
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
43
44.
СТРУКТУРА ДЕФОРМИРОВАННЫХПОЛУФАБРИКАТОВ ДО И ПОСЛЕ
ТЕРМИЧЕСКОЙ ОБРАБОТКИ
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
44
45. Волокнистая (а) и рекристаллизованная (б) зеренная структура (СМ)
а09.02.2017
б
Курс “Структура и свойства цветных металлов и сплавов“
45
46. Карта структуры после многократной прокатки методом анализа картины обратно рассеянных электронов EBSD в СЭМ
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
46
47. ТЕКСТУРЫ ДЕФОРМАЦИИ
1. В катаных листах - двойная текстура прокатки {110}<112> (основная втехническом Al) и {112}<111> (основная в сплавах).
2. После прессования, волочения, прокатки прутков и проволоки
круглого сечения образуется двойная аксиальная текстура <111> и
<100>.
3. В прессованных полосах и тонкостенных профилях – текстура
прокатки + аксиальная при больших отношениях толщины к
ширине.
4. В трубах, получаемых прессованием, прокаткой и волочением, «цилиндрическая» текстура (текстура прокатки после разрезки
трубы и разворота ее в плоскость).
5. В осаженных прутках – аксиальная текстура <110>
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
47
48. Диаграмма структурных состояний закаленного деформируемого сплава АК8 в зависимости от температуры и скорости горячей деформации при оса
Диаграмма структурных состояний закаленногодеформируемого сплава АК8 в зависимости от
температуры и скорости горячей деформации при
осадке
прессование
штамповка
прокатка
ковка
09.02.2017
1 - рекристаллизации
нет;
2- полная
рекристаллизация;
3- рекристаллизация
начинается после
деформации;
4- смешанная структура
Курс “Структура и свойства цветных металлов и сплавов“
48
49. Субструктура (Al) после возврата и строчечность частиц в волокнистом полуфабрикате
0,5 мкм09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
49
50. Дисперсоиды в конечной структуре деформированных полуфабрикатов (ПЭМ)
1 мкм1мкм
200 нм
200 нм
51. Термомеханическая обработка алюминиевых сплавов
ВТМО – горячая деформация с получениемполигонизованной структуры, сохраняющейся после
закалки или отжига – упрочнение по сравнению с
рекристаллизованным состоянием (Al) («прессэффект» или «структурное упрочнение»)
НТМО – холодная деформация (прокатка) после
закалки перед старением
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
51
52. Cпособы получения нанокристаллической структуры -введением при распаде (Al) наночастиц фаз-упрочнителей (в литейных и деформируемых сплава
Cпособы получениянанокристаллической структуры
-введением при распаде (Al) наночастиц фазупрочнителей
(в литейных и деформируемых сплавах)
-путем интенсивной пластической
деформации разными способами:
кручение под гидростическим
давлением (КГД)],
равноканальное угловое прессование
(РКУП),
многократная прокатка,
механическое легирование
и другие для получения наноразмерного зерна
в (Al)
53.
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
53
54. Интенсивная пластическая деформация (ИПД)
1ln(1)
Интенсивная пластическая
деформация (ИПД)
Величина деформации в работах по ИПД
рассчитывается по формуле ε=-ln(1- /1), где для
листов – это разность исходного размера (диаметра
или толщины) заготовки и размера после деформации.
Например, если исходная заготовка имела толщину 10
мм, а в результате прокатки мы получили из нее лист
толщиной 1 мм, то
ε=-ln{1- (10-1)/10}=ln(0,1)=2,3.
При ИПД ε может достигать 3-4 и более за один проход
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
54
55. Схемы РКУП и КГД
РКУП - многократное продавливание образца черезканал без изменения его
формы
.
КГД-деформация за счет сил трения по
поверхности дискового образца
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
55
56. Промышленные литейные алюминиевые сплавы
Базовые системы легирования,маркировка.
Химический и фазовый состав.
Особенности структуры и свойств
силуминов и литейных сплавов на
основе систем Al – Mg, Al – Cu и Al – Zn
– Mg
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
56
57. Системы обозначения промышленных литейных алюминиевых сплавов в России и США
Базовая системаAl-Cu
Al-Si-Cu, Al-Si-Mg,
Al-Si-Cu-Mg
Al-Si
Al-Mg
Al-Zn
Al-Sn
09.02.2017
США (АА)
2XX.0 (224.0)
3XX.0 (356.0)
4XX.0 (413.0)
5XX.0 (514.0)
7XX.0 (710.0)
8XX.0 (850.0)
Россия (ГОСТ 1583-89)
(АМ5)
(АК12М2МгН)
(АК12)
(АМг5К)
Курс “Структура и свойства цветных металлов и сплавов“
57
58. Сравнительная характеристика свойств литейных сплавов
СистемаПрочн.
Кор.
стойк.
Лит.
св-ва
Свар.
Al-Si
1
2
1
2
3
3
Al-Si-Mg
2
1-2
1
2
3
3
Al-Si-Cu
2
1-2
2
1
3
3
Al-Si-Cu-Mg
2-3
1
2
1
2-3
3
Al-Cu
3
3
3
1
1
2
Al-Mg
1-2
3
1
3
2
3
09.02.2017
Пласт. Жаропроч.
Курс “Структура и свойства цветных металлов и сплавов“
58
59. Гарантируемые механические свойства силуминов по ГОСТ 1583-93
Маркисплавов
Способ
литья
Состояние
АК7ч
К
Т6
235
1
70
АК9ч
З, К
Т6
230
3
70
АК8М3ч
К
Т5
390
4
110
АК12ММг
Н
К
Т6
215
0,7
100
09.02.2017
в,МПа, %
Курс “Структура и свойства цветных металлов и сплавов“
НВ
59
60. Механические свойства литейных сплавов на базе систем Al–Cu и Al–Mg по ГОСТ 1583-93
СплавАМ5
АМ4,5Кд
АМг6л
АМг6лч
АМг10(АЛ27)
09.02.2017
Способ
литья
в, МПа
, %
НВ
З
333
4
90
К
333
4
90
К
490
4
120
З
190
4
60
К
220
6
60
З, К
230
6
60
З
200
5
60
К
240
10
60
З, К
250
10
60
З, К
320
12
75
Курс “Структура и свойства цветных металлов и сплавов“
60
61. Промышленные деформируемые сплавы
Базовые системы легирования, маркировка,химический и фазовый состав
Термически неупрочняемые сплавы на основе
систем Al – Fe – Si, Al – Mg, Al – Mn,
особенности их структуры и свойств.
Термически упрочняемые сплавы на основе
систем Al – Cu, Al – Mg, Al – Mg – Si,
Al – Cu – Mg, Al – Zn – Mg – Cu, Al – Mg – Cu –
Li.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
61
62. Системы обозначений промышленных деформируемых алюминиевых сплавов в России и США
Базоваясистема
>99.0% Al
Al-Cu
Al-Mn
Al-Si
Al-Mg
Al-Mg-Si
Al-Zn
Остальные
09.02.2017
США (АА)
1ХХX
2XXX
3XXX
4XXX
5XXX
6XXX
7XXX
8XXX
(1180)
(2024)
(3005)
(5086)
(6010)
(7075)
(8111)
Россия (ГОСТ 4784-74)
Цифровая – (буквенная)
10YY –
(АД1)
11YY – (Д16, АК4-1)
14YY – (АМц)
15YY – (АМг6)
13YY – (АВ, АД31)
19YY –
(В95)
–
- (АЖ0.8)
Курс “Структура и свойства цветных металлов и сплавов“
62
63. Концентрация основных легирующих элементов в промышленных деформируемых сплавах
Cu, %Mg, %
Zn, %
Si, %
Li, .%
Al-Cu-Mg
3-5
0,5-2
-
-
-
Al-Mg-Si
-
0,3-1,2
-
0,3-1,2
-
Al-Zn-Mg
-
1-3
3-6
-
-
Al-Cu-Mg-Si
1-5
0,3-1,2
-
0,3-1,2
-
Al-Zn-Mg-Cu
0,5-3
1-3
5-9
-
-
Al-Li-Cu-Mg
0–4
0-5
–
–
1–3
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
63
64. Сравнительная характеристика свойств деформируемых сплавов
Базоваясистема
Прочн. Пласт. Жароп.
Корр.
Дефор.
Свар.
Al-Mg
1-2
3
1
3
2
3
Al-Cu
3
3
3
1
2
2
Al-Mg-Si
2
3
2
3
3
2
Al-Cu-Mg
3
3
2
1
3
1
Al-Zn-Mg
1
2
1
3
3
2
Al-Zn-Mg-Cu
3
2
1
2
2
1
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
64
65. Обозначение некоторых состояний для деформируемых алюминиевых сплавов
Вид термообработкиОбозначение в
РФ1)
Обозначение
в США2)
Без термообработки, без контроля наклепа
–
F
Отжиг для полного снятия наклепа
М
O
Нагартованное состояние без термообработки
Н
H1
Нагартованное и частично отожженное состояние
Н1, Н2, Н3
H2
Нагартованное и стабилизированное состояние
–
Н3
Закалка после деформации плюс естественное
старение
T
T4
Закалка после деформации плюс старение на
максимальную прочность
T1
T6
Закалка после деформации плюс перестаривание
Т2, Т3
T7
Закалка после деформации, холодная деформация,
искусственное старение (НТМО)
T1Н
T8
1)
русские буквы,
09.02.2017
2)
латинские буквы
Курс “Структура и свойства цветных металлов и сплавов“
65
66. Типичные механические свойства термически неупрочняемых алюминиевых деформируемых сплавов
СплавВид полуфабриката
Состояние
в,
МПа
0,2,
МПа
, %
АД00
Лист
М
60
–
28
АД1
Лист
Н
145
–
4
АМц
Лист
Н
185
–
4
АМг2
Лист
М
165
–
18
АМг2
Профиль
М
225
60
13
АМг3
Лист
М
195
100
15
АМг6
Лист
М
155
155
15
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
66
67. Типичные механические свойства термически упрочняемых алюминиевых деформируемых сплавов
СплавВид полуфабриката
Состояние
в, МПа
0,2, МПа
, %
Д16
Лист
Т
440
290
11
Д20
Поковка
Т1
375
255
10
АК8
Пруток
Т1
450
–
10
АВ
Лист
М
145
–
20
АВ
Профиль
Т1
294
225
10
АД31
Пруток
Т1
195
145
8
В95
Пруток
Т1
510
420
6
В96ц
Поковка
Т1
590
540
4
1915
Лист
Т
315
195
10
АК4-1
Пруток
Т1
390
315
6
1420
Профиль
Т1
412
275
7
1450
Лист
Т1
490
430
4
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
67
68. Пример билета к контрольной работе
1.2.
3.
4.
5.
В какой области диаграммы состояния
находятся составы алюминиевых сплавов с
хорошими литейными свойствами?
Какие процессы идут при закалке
деформированных полуфабрикатов из
алюминиевых сплавов?
Модифицирование структуры литейных
алюминиевых сплавов
Структура и свойства дуралюминов
Безмедистые силумины
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
68
69. Тугоплавкие металлы и сплавы
70. План раздела
Тугоплавкие металлы, их распространенность в земной коре,применение. Металлы «большой четверки».
Общие особенности электронной и кристаллической структуры
тугоплавких металлов с ОЦК решеткой.
Физические свойства.
Химические свойства. Способы защиты тугоплавких металлов от
взаимодействия с газами воздуха
Состав защитных покрытий и способы их нанесения на тугоплавкие
металлы и сплавы.
Механические свойства: проблемы хладноломкости и жаропрочности
Принципы легирования тугоплавких металлов с целью создания
жаропрочных сплавов.
Промышленные сплавы.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
70
71. Максимальные рабочие температуры жаропрочных сплавов на разной основе
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
71
72. Особенности электронной структуры
Тугоплавкие металлы IV-VII групп – переходныеd-элементы
V и Cr расположены в I-ом большом периоде, Zr,
Nb и Mo во II-ом, Ta, W, Nb и Re – в III-ем
Соответственно у них не полностью заполнены
3d-, 4d- и 5d-уровни, а количество электронов на
внешних уровнях почти одинаково
В результате кристаллическая структура у всех
этих металлов тоже близка
Как минимум одна модификация имеет ОЦК
решетку со всеми ее особенностями
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
72
73. Распространенность в земной коре, кристаллическая структура и некоторые физические свойства тугоплавких металлов
Плотность,г/см3
Удельное
электросопротивление,
мкОм·см
Температура
перехода
в сверх проводящее
состояние,
К
Поперечное
сечение
захвата
тепловых
нейтронов,
барны
Металл
Содержание
в
земной
коре,
%
Тип
кристаллической
решетки
Цирконий
0,022
-ГП
-ОЦК
1852
6,5
42
0,7
0,18
Ванадий
0,0150
ОЦК
1900
6,14
24,8
5,13
4,98
Ниобий
0,0024
ОЦК
2468
8,58
12,7
9,22
1,15
Тантал
0,00021
ОЦК
3000
16,65
12,4
4,38
21
Хром
0,020
ОЦК
1875
7,19
12,8
-
3,1
Молибден
0,0015
ОЦК
2625
10,2
5,78
0,9-0,98
2,7
Вольфрам
0,0069
ОЦК
~3400
19,35
5,5
0,05
19,2
Рений
1·10-7
ГП
3180
21,02
19,14
1,7
86
Медь
0,007
09.02.2017
Температура плавления, 0С
Курс “Структура и свойства цветных металлов и сплавов“
73
74. Температура плавления переходных металлов трех длинных периодов
Максимум Тпл – при6 (d+s)-электронах
когда максимальна
прочность сил межатомной связи
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
74
75. Химические свойства Схемы зависимости скорости окисления от времени при постоянной температуре
Покисление начинаетСильное
р 400-5000С.
при т-рах
Причины
и линейного окислен
-низкая Тпл и Ткип оксида
(279 и 3630С у Re2O7, 795 и
14600С у МоО3),
-рыхлая крист. решетка, силь
отличающаяся от маталла
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
75
76. Взаимодействие с водородом и азотом
С водородом металлы VI-группы и рений втвердом состоянии не взаимодействуют
Металлы IV- и V-групп активно
взаимодействуют с водородом выше 250-3000С
с образованием гидридов
С азотом взаимодействуют все тугоплавкие
металлы, особенно IV группы, меньше других хром
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
76
77. Защитные атмосферы и покрытия
Защитные атмосферы: вакуум, аргон,водород (для W и Mo)
Защитные покрытия получают
хромированием, силицированием,
оксидированием (Al2O3, ThO2, ZrO2),
многослойным вакуумным напылением (Cr,
Si) с последующим диффузионным
отжигом
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
77
78. Механические свойства 2 основные проблемы –хладноломкость и жаропрочность Температурные зависимости относительного сужения
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
78
79. Природа хладноломкости ОЦК металлов
1.Роль примесей, особенно образующих растворывнедрения
-предельная растворимость
-сегрегация на дислокациях
-равновесная сегрегация на границах
зерен
-образование частиц избыточных фаз
2. Влияние дислокационной структуры
3. Влияние зеренной структуры
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
79
80. Растворимость углерода, азота и кислорода в тугоплавких металлах VА и V1А-подгрупп при комнатной температуре
МеталлРастворимость ▪ 10-4 , %
углерода
азота
кислорода
Молибден
0,1 -1
1
1
Вольфрам
< 0,1
<0,1
<1
Ниобий
100
200
1000
Тантал
70
1000
200
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
80
81. Схемы структур тугоплавких ОЦК металлов в различных состояниях а – г -структуры в световом микроскопе; д – ж -дислокационная структура фол
Схемы структур тугоплавких ОЦК металлов в различныхсостояниях
а – г -структуры в световом микроскопе;
д – ж -дислокационная структура фольги в электронном микроскопе;
а – литое состояние; б – деформированное;
в – рекристаллизованное состояние; г – монокристалл;
д – гомогенное распределение дислокаций;
е – ячеистая структура; ж – полигонизованная структура
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
81
82. Схемы изменения температуры хрупко -вязкого перехода тугоплавких металлов (Тхр) при легировании
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
82
83. Способы уменьшения хладноломкости
Снижение концентрации примесейвнедрения
Устранение сетки высокоугловых границ
Создание полигонизованной структуры
Измельчение зерна
Легирование рением и химически
активными элементами
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
83
84. Температурные зависимости предела прочности (а) и удельной прочности (б) тугоплавких металлов
а09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
б
84
85. Влияние легирования на жаропрочность
Твердорастворное упрочнение добавками,повышающими или слабо снижающими
солидус металла – основы, т.е. другими
тугоплавкими элементами
Фазы – упрочнители: чаще всего карбиды, а
также нитриды, оксиды, бориды
Способы введения частиц фаз-упрочнителей –
порошковая металлургия,
- «слиточная» технология
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
85
86. Диаграмма состояния Ti – Mo
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
86
87. Диаграмма состояния Mo – W
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
87
88. Диаграмма состояния Zr – Nb
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
88
89. Схема конструирования состава жаропрочных сплавов на основе металлов «большой четверки»
Ме-основа (Мо, W, Nb, Ta) + растворимыедобавки для повышения жаропрочности (те
же металлы) и низкотемпературной
пластичности (Ti, Zr, Hf, РЗМ)+ добавки,
образующие фазы –упрочнители (С и
другие металлоиды)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
89
90. Температурные зависимости предела прочности вольфрамовых сплавов
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
90
91.
Расшифровка кривых на слайде 94Номер
кривой
Сплав
Метод получения
Состояние или обработка
1
100% W
Порошковая металлургия
Деформированный лист
2
W 100%W
-”-
Кованный пруток
3
W +10%Mo
-”-
-”-
4
W +15%Mo
Дуговая плавка
-”-
5
W +20%Mo
Электроннолучевая плавка
12050С, 1 час
6
W +25%Mo
Порошковая металлургия
Кованный пруток
7
W +30%Mo
Электроннолучевая плавка
12050С, 1 час
8
W +50%Mo
Порошковая металлургия
Кованный пруток
9
W +1%Th02
-”-
-”-
10
W +2%Th02
-”-
-”-
11
W +0,12%Zr
Дуговая плавка
Прессование, ковка
12
W +0,57%Nb
-”-
-”-
13
W +0,88%Nb
-”-
-”-
14
W +0,38%TaC
Порошковая металлургия
Ковка + 10000С, ½ ч
15
W +1.18%Нf + 0,086%С
-”-
Прессование, ковка
16
W +0.48%Zr + 0,048%С
-”-
-”-
17
Cплав ВВ2
Дуговая плавка
-”-
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
91
92. Химический состав и свойства молибденовых сплавов в отожженном состоянии
Среднее содержание, %Температура
начала
рекристаллизации, 0С
σв при
1315 0С,
МПа
σ100
при
1315 0С,
МПа
Марка
сплава
Ti
Zr
W
Nb
C
Mo
-
-
-
-
<0.005
1100
150
30
ЦМ-5
-
0,45
-
-
0,05
1600
360
140
ЦМ-2А
0,2
0,1
-
-
≤0,004
1300
160 при
1400 0С
65
до 0,6
-
≤0,01
1300
190 при
1400 0С
90 при
1200 0С
-
1,4
0,3
1650
380
265
ВМ-1
ВМ-3
09.02.2017
до 0,4 0,15
1
0,45
Курс “Структура и свойства цветных металлов и сплавов“
92
93. Химический состав и свойства ниобиевых сплавов
Плотность,г/см3
Температура
начала
рекристаллизации, 0С
Предел
прочности в
отожженном
состоянии
при 12000С
σв, МПа
Группа
сплавов
Марка
сплава
Среднее
содержание
легирующих
элементов, %
Малопрочные
ВН-2
4,5 Mo
8,6
1000
190
ВН-2А
4 Mo; 0.7Zr;<0,08C
8,65
1200
240
ВН-3
4,6Mo; 1.4Zr; 0.12C
8,6
1200
250
ВН-4
9,5Mo; 1,5Zr;
0,3C; 0,03Ce; La
-
1400
2500
Среднепрочные
Высокопрочные
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
93
94. Радиоактивные металлы
95. План раздела
Радиоактивный распад и цепная ядерная реакция.Ядерный реактор.
Уран.
Физические, химические и механические свойства урана.
Радиационное повреждение урана. Радиационный рост
урана.
Газовое распухание урана и способы борьбы с ним.
Размерная нестабильность урана при работе реакторов.
Основные легирующие элементы.
Сплавы урана
Плутоний и его сплавы
Торий и его сплавы
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
95
96. Состав ядер атомов
-23радиоактивных металла, используются в основном U, Pu и Th.
-Ядро состоит из нуклонов – положительно заряженных протонов и
нейтронов, имеющих примерно одинаковую массу.
-Число протонов Z (положительный заряд ядра) равно числу электронов.
-Заряд ядра Z равен суммарному числу протонов (или электронов)
-Число нуклонов (массовое число) М = Z + N (N – число нейтронов).
-У многих элементов при одном Z несколько значений N и М
-Изотопы – атомы с одинаковым Z, но разным М.
-Нуклоны в ядре связаны ядерными силами, на 6 порядков большими,
чем электростатические силы отталкивания протонов.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
96
97. Распад и синтез ядер При увеличении Z ядерные силы сначала растут, а потом у тяжелых элементов уменьшаются. Синтез легких и распад тяжелых я
Распад и синтез ядерПри увеличении Z ядерные силы сначала растут, а потом у тяжелых
элементов уменьшаются.
Синтез легких и распад тяжелых ядер сопровождается выделением большой
энергии.
Условие стабильности ядра:
M
Z
2
1,98067 0, 0149624 M 3
Дефект массы при потере или приобретении энергии: m = E/c2,
где E – величина выделяющейся или приобретаемой энергии;
c – скорость света.
При образовании в результате синтеза ядер 1 кг гелия m = 80 г. При этом
выделяющаяся энергия E = 4,47 ·1028 МэВ (как при сгорании 20 000 т угля).
При распаде ядер тяжелых элементов также образуется огромная энергия (при
распаде ядер 1 кг U в 8 раз меньшая, чем при синтезе 1 кг He)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
97
98. Разновидности реакций распада ядер радиоактивных изотопов (естественная радиоактивность)
1.2.
3.
- распад с выделением –частицы (ядра гелия с
М=4 и Z=2). При этом образуется новое ядро.
Например, 226Ra88 4 2 + 222Rn86.
Позитронный или +-распад (позитрон – 0e+1)
Например, 30P15 0e+1 + 30Si14 + 0 0 ,
где
-нейтрино.
К – захват. Ядро захватывает электрон с оболочки
своего атома (чаще всего с К –оболочки), который
соединяется с протоном, образуя нейтрон.
Например, 55Fe26 + 0e-1 54Mn25 + 1n0.
При избытке нейтронов в ядре они распадаются: 1n0
1P1 + 0e-1 +0 0.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
98
99. Реакции при бомбардировке ядер частицами
Ядерные реакции – поглощение частиц –бомбардиров ядрамиЕсли частица не поглощается ядром, то говорят о рассеянии
Если частица поглощается ядром, то образуется короткоживущее
(<10-16 сек) ядро, превращающееся в другое, испуская одну или
несколько частиц
Возможно образование «возбужденных» ядер, которые отдают
свой избыток энергии в виде электромагнитного излучения
Во всех ядерных реакциях Z и M остаются неизменными, а в
результате реакции выделяется или поглощается энергия
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
99
100. Эффективное поперечное сечение бомбардируемых ядер (характеризует вероятность прохождения ядерной реакции)
Эффективное поперечное сечениебомбардируемых ядер (характеризует
вероятность прохождения ядерной
реакции)
P = F N d ,
где P – число ядерных процессов;
F – число частиц-снарядов;
d – толщина фольги–мишени;
N – число ядер.
-Размерность – барны (1 барн = 10-24 см2).
-Наилучшие частицы-бомбардиры – нейтроны, которые
легко можно получать в реакторах и для которых не
существует кулоновского барьера.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
100
101. Схема зависимости энергии связи ядра на 1 нуклид (Q/М) от массового числа М
Реакциейделения
можно
управлят
С ядер
Синтез
и
(идет
в термоядерных
реакциях) пока
неуправляем
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
101
102. Схема зависимости % выхода образующихся при делении ядер урана и тория от массового числа М
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
102
103. Цепная ядерная реакция
При делении ядер в результате их бомбардировкинейтронами выделяется энергия и образуются
нейтроны деления – мгновенные (10-15 сек) и
запаздывающие (0,114-54,3 сек после деления)
■ Образовавшиеся нейтроны расщепляют др. ядра,
в результате образуется еще больше нейтронов и
идет цепная ядерная реакция, обусловленная
тем, что вместо каждого потерянного в процессе
деления ядер нейтрона образуется в среднем
больше, чем один нейтрон
■ Управлять цепной реакцией можно только
благодаря наличию запаздывающих нейтронов
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
103
104. Ядерный реактор
Ядерный реактор – аппарат, в которомпроисходит управляемый процесс деления
ядер.
Для непрерывного прохождения цепной
ядерной реакции деления надо компенсировать
потери нейтронов – число образующихся при
делении ядер нейтронов должно быть равно
или больше начального количества нейтронов
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
104
105. Принципиальная схема простейшего ядерного реактора (с массой, близкой к критической)
Коэффициентразмножения
K = · f ·n,
где - доля непоглощенных
первичных нейтронов,
f – доля нейтронов от доли, которые
вызвали деление,
n- число новых нейтронов,
образовавшихся при одном делении
К должен быть равен или больше
1 (но немного – до ~1,01), чтобы
шла управляемая цепная
реакция.
Если К=2, то произойдет
атомный взрыв через 10-6 сек
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
105
106. Принципиальная схема гетерогенного ядерного реактора
1 – урановые стержни (ТВЭЛы);2 – замедлитель (с
минимальным P и атомным
весом – графит,Be);
3 – отражатель (из материалов,
подобных замедлителю);
4 – защита;
5 – регулирующий стержень
(с большим P)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
106
107. Принципиальная схема ТВЭЛа (поперечное сечение)
1 – пруток ядерногогорючего;
2 – внутренняя
оболочка;
3 – внешняя оболочка;
4 – канал для
теплоносителя
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
107
108. УРАН Изотопный состав урана и реакции при захвате нейтронов ядрами 238U
Изотопы урана:234U
238U
(0,006%), 235U (0,712%), 238U (99,28%)
делится только быстрыми нейтронами с большой энергией. При
взаимодействии с тепловыми нейтронами:
+ n 239U92 +
239U 239Np + e
92
93
-1
239Np 239Pu + 0e
93
94
-1
238U
238U
235U
09.02.2017
92
Значительного выделения энергии в этих реакциях не происходит.
является топливным сырьем для получения Pu.
является легко делящимся тепловыми нейтронами изотопом
Курс “Структура и свойства цветных металлов и сплавов“
108
109. Физические, химические свойства и полиморфные превращения в уране
Температура плавления урана 1132 0С.(ОЦК) – модификация U стабильна при охлаждении до 764 775
0С.
-фаза (сложная тетрагональная решетка) – существует в
диапазоне от 7750 665 0С
0
(ромбическая решетка) – ниже 665 С
Переход β →α происходит с сильным уменьшением объема
(плотность увеличивается с 18,1 до 19,1 г/см3), это
вызывает большие внутренние напряжения
Низкая электро – и теплопроводность
(= 30 мкОм см)
■ Высокая химическая активность на воздухе (вплоть до
самовозгорания порошка), в воде и многих др. средах, с
жидкометаллическими теплоносителями взаимодействует слабо
- Природный уран радиационно практически безопасен
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
109
110. Влияние температуры на механические свойства урана, прокатанного в – области с последующим быстрым охлаждением
Влияние температуры на механическиесвойства урана, прокатанного в – области с
последующим быстрым охлаждением
При комнатной т-ре
у чистого (99,95%)
урана σв=300-500
МПа, =4-10%
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
110
111. Изменение формы и размеров U при облучении и ТЦО
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
111
112. Радиационное повреждение – изменение формы и размеров прутков ядерного горючего, повышение твердости, охрупчивание, образование пор и тр
Радиационное повреждение –изменение формы и размеров прутков ядерного горючего, повышение
твердости, охрупчивание, образование пор и трещин, шероховатость
поверхности
Причины радиационного «роста»:
1) смещение атомов из положений равновесия,
2) внедрение продуктов деления в кристаллическую
решетку,
3) возникновение «термических пиков»,
4) анизотропия кристаллической решетки
Свеллинг – газовое распухание при высоких
температурах (>400 0С) из-за образования при
делении ядер ксенона и криптона
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
112
113. Размерная нестабильность в условиях многократных теплосмен
Наблюдается при наличии сильной текстуры,устранение текстуры устраняет
формоизменение
Чем крупнее зерно, тем меньше рост, но
рельефней получается поверхность
Структурные изменения: рекристаллизация,
полигонизация, образование пор
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
113
114. Зависимость изменения длины уранового стержня от числа циклов нагрева и охлаждения 100 0С 500 0С 1 – после прокатки при 300 0С и отжига при 575 0С;
Зависимость изменения длины уранового стержня от числациклов нагрева и охлаждения 100 0С 500 0С
1 – после прокатки при 300 0С и отжига при 575 0С;
2 – после прокатки при 600 0С и отжига при 575 0С; 3 – после прокатки при 600
0С и закалки из – области
СС
кк
о
р
о
с
т
ь
Скорость
роста падает
С
с ослаблением
к
текстурованности
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
114
115. Сплавы урана
Сплавы с α-структурой –малолегированные (10-2 % Al, Fe, Si),
сплавы с Mo, Zr, Nb (до 10%) – отсутствие
текстуры, мелкое зерно, дисперсные
частицы
Сплавы с γ-структурой (ОЦК) с Mo, Zr, Nb
(более 10%) –уменьшенное
формоизменение, повышенная
пластичность и коррозионная стойкость
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
115
116. Керамическое и дисперсионное ядерное горючее (ЯГ)
Керамическое ЯГ – соединения U и др.радиоактивных металлов с металлоидами (O, C,
N) – получают методами порошковой
металлургии
Дисперсионное ЯГ – это композиты с
дискретными частицами соединений
радиоактивных металлов в нерадиоактивной
матрице (металлической, графитовой или
керамической)
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
116
117. Фазовая диаграмма системы U – Mo
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
117
118. Фазовая диаграмма системы U – Zr
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
118
119. Плутоний и его сплавы Полиморфизм плутония
Полиморфныепревращения
в плутонии
Tпп,
0С
Кристаллическая решетка
аллотропических
модификаций Pu
Плотность,
г/см3
472
- ОЦК
16,5
450
- объемноцентрированная
16
тетрагональная
310
- ГЦК
15,9
218
- гранецентрированная
17,1
ромбическая
119
- объемноцентрированная
17,8
моноклинная
- простая моноклинная
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
19,8
119
120. Свойства плутония
■ -Pu – еще более химически активен, чем уран,радиационно опасен из-за - и -излучения,
обладает очень большим КТР и электросопротивлением
(145 мкОм.см);
-предел прочности 350-400 МПа, <1%.
■ -Pu с ГЦК-решеткой пластичен, изотропен по свойствам,
имеет положительный температурный коэффициент
электросопротивления и отрицательный ТКР;
■ большие объемные изменения при полиморфных
превращениях;
■ невозможность использования чистого Pu в ядерных
реакторах.
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
120
121. Салавы плутония
Сплавы Pu c Al (на основе Al – дисперсионное ЯГ – сл.128)Сплавы с переходными металлами (Zr, Ce, Fe)
Сплавы Pu-U, Pu-Th и Pu-U-Mo для реакторов на
быстрых нейтронах
Фиссиум – сплавы U-Pu со смесью продуктов
деления (в основном Mo и Ru)
Сплавы Pu с Fe, Ni, Co с низкой Тпл для
жидкого ядерного горючего
■ Сплавы Pu c Ga – стабилизация -фазы сильно
уменьшает объемные изменения
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
121
122. Температурные зависимости изменения длины Pu и его сплавов с Ga
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
122
123. Растворимость некоторых добавок в и модификациях Pu
Растворимость некоторых добавок ви модификациях Pu
Фазы
Легирующий
элемент
Алюминий
13 – 16
12
Цинк
6
3–6
Церий
24
14
Торий
4
4–5
Титан
4,5
8
Железо
1,4 – 1,5
3
Цирконий
70 – 72
Полная
Уран
1
Полная
09.02.2017
Влияние легирующего
элемента на нижнюю
границу области
Повышает
Курс “Структура и свойства цветных металлов и сплавов“
123
124. Фазовая диаграмма системы Pu – Al
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
124
125. Фазовая диаграмма системы Pu – Zr
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
125
126. Фазовая диаграмма системы Pu – U
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
126
127. Фазовая диаграмма системы Pu – Fe
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
127
128. Торий и его сплавы Реакции превращения 232Th в 233U
Торий и его сплавыРеакции превращения
232Th
232Th +
+
n
90
90
233Pa
232Th
в 233U
0e
+
91
-1
233U
92
+e
Т-ра плавления технического Th 1690 0С.
При 1400 0С -Th с ГЦК решеткой переходит в -Th с ОЦК решеткой.
Плотность - Th 11,65 г/см3,
Удельное электросопротивление 20-30 мкОм·см
КТР 11,7 10-6 град-1 – в несколько раз меньше, чем у U
Имеет хорошую пластичность и изотропность свойств благодаря ГЦК
решетке, но малопрочен (HV 40-80)
Высокая жаропрочность
Химическая активность ниже, чем у урана
Используется чаще всего в виде сплавов с ураном при повышенной
концентрации 235U
09.02.2017
Курс “Структура и свойства цветных металлов и сплавов“
128
129. Фазовая диаграмма системы Th – U
09.02.2017Курс “Структура и свойства цветных металлов и сплавов“
Цель работы: изучение диаграмм фазового равновесия и фазовых превращений в бинарных сплавах алюминия с другими элементами.
Необходимое оборудование, приспособления, инструмент, материалы: муфельные печи, твердомер ТК-2М, образцы дуралюминов, стенд «Микроструктуры цветных сплавов», металлографический микроскоп.
Теоретические сведения
Алюминий является важнейшим металлом, широко применяемым для изготовления разнообразных алюминиевых сплавов.
Цвет алюминия серебристо-белый со своеобразным тусклым оттенком. Кристаллизуется алюминий в пространственной решетке гранецентрированного куба, аллотропических превращений у него не обнаружено.
Алюминий имеет малую плотность (2,7 г/см 3), высокую электропроводность (составляющую около 60 % электро-проводности чистой меди) и значительную теплопроводность.
В результате окисления алюминия кислородом воздуха на его поверхности образуется защитная оксидная пленка. Наличием этой пленки объясняется высокая коррозионная стойкость алюминия и многих алюминиевых сплавов.
Алюминий достаточно стоек в обычных атмосферных условиях и против действия концентрированной (90-98 %) азотной кислоты, однако он легко разрушается при действии большинства других минеральных кислот (серная, соляная), а также щелочей. Он обладает высокой пластичностью как в холодном, так и горячем состоянии, хорошо сваривается газовой и контактной сваркой, но плохо обрабатывается резанием и отличается низкими литейными свойствами.
Для прокатанного и отожженного алюминия характерны следующие механические свойства: в = 80-100 МПа, = 35-40 %, НВ = 250…300 МПа.
При нагартовке прочность алюминия повышается, а пластичность снижается. Соответственно по степени деформации различают отожженный (АД-М), полунагартованный (АД-П) и нагартованный (АД-Н) алюминий. Отжиг алюминия для снятия наклепа проводится при 350…410 С.
Чистый алюминий находит разнообразное применение. Из технического алюминия АД1 и АД, содержащего соответственно не менее 99,3 и 98,8 % Al, изготовляют полуфабрикаты – листы, трубы, профили, проволоку для заклепок.
В электротехнике алюминий служит для замены более дорогой и тяжелой меди при изготовлении проводов, кабелей, конденсаторов, выпрямителей и т. п.
Важнейшими элементами, вводимыми в алюминиевые сплавы, являются медь, кремний, магний и цинк.
Алюминий с медью образует твердые растворы переменной концентрации. При температуре 0 С растворимость меди в алюминии равна 0,3 %, а при температуре эвтектики 548 С она увеличивается до 5,6 %. Алюминий и медь в соотношении 46:54 образуют стойкое химическое соединение CuAl 2 .
Рассмотрим состояние сплавов алюминия с медью в зависимости от их состава и температуры (рис. 1). Линия CDE на диаграмме представляет собой линию ликвидуса, а линия CNDF является линией солидуса. Горизонтальный участок линии солидуса NDF называется также эвтектической линией.
Линия MN показывает переменную по температуре растворимость меди в алюминии. Следовательно, линия MN является границей между ненасыщенными твердыми растворами и растворами насыщенными. Поэтому эту линию часто называют также линией предельной растворимости.
В области I любой сплав будет представлять собой однородный жидкий раствор алюминия с медью, т. е. AlCu.
Р ис.
1. Диаграмма состояния системыAl–CuAl 2
ис.
1. Диаграмма состояния системыAl–CuAl 2
В областях II и III сплавы будут находиться частично в жидком и частично в твердом состояниях.
В области II
твердой фазой будет твердый раствор
меди в алюминии, а жидкой – жидкий
раствор алюминия и меди, т.е. Al(Cu)
+ (Al Cu),
если твердый раствор ограниченной
растворимости меди в алюминии условимся
обозначать как Al(Cu).
Cu),
если твердый раствор ограниченной
растворимости меди в алюминии условимся
обозначать как Al(Cu).
В области III
жидкой фазой будет являться также жидкий
раствор алюминия и меди, а твердой –
металлическое соединение CuAl 2 ,
т. е.
 +
(Al
+
(Al Cu).
Индекс «I»
(первичный) показывает, что CuAl 2
образовалось при кристаллизации из
жидкого состояния.
Cu).
Индекс «I»
(первичный) показывает, что CuAl 2
образовалось при кристаллизации из
жидкого состояния.
В остальных областях полностью затвердевшие сплавы будут иметь следующее строение:
В области IV – однородный твердый раствор меди в алюминии, т. е. Al(Cu);
В области V
– твердый раствор меди в алюминии и
вторичный
 ;
;
В области VI
– твердый раствор меди в алюминии,
вторичный CuAl 2
и эвтектика, т.е Al(Cu)
+ +Al(Cu)
+ CuAl 2 ;
+Al(Cu)
+ CuAl 2 ;
В области VII
– первичный CuAl 2
и эвтектика, т. е.
 +Al(Cu)
+ CuAl 2 .
+Al(Cu)
+ CuAl 2 .
Эвтектика этих сплавов представляет собой особую механическую смесь чередующихся мельчайших кристаллов твердого раствора меди в алюминии и металлического соединения CuAl 2 , т.е. Al(Cu) + CuAl 2 .
Все сплавы системы Al – CuAl 2 по структуре и концентрации можно разделить на четыре группы:
1-я группа содержит меди от 0 до 0,3 %;
2-я группа содержит меди от 0,3 до 5,6 %;
3-я группа содержит меди от 5,6 до 33,8 %;
4-я группа содержит меди от 33,8 до 54 %.
Рассмотрим строение сплавов системы Al – CuAl 2 .
На рис. 2, а показана структура сплава первой группы, состоящая из зерен твердого раствора меди в алюминии. Структура сплава второй группы приведена на рис. 2, б : видны зерна твердого раствора меди в алюминии и кристаллы вторичного CuAl 2 ,
Структура доэвтектического сплава (твердый раствор меди в алюминии, кристаллы вторичного CuAl 2 и эвтектика) приведена на рис. 2, в . Структура эвтектического сплава – эвтектика, состоящая из мельчайших кристалликов твердого раствора меди в алюминии и CuAl 2 дана на рис. 2, г . На рис. 2, д приведена структура заэвтектического сплава, состоящая из первичных кристаллов CuAl 2 и эвтектики.
В сплавах, содержащих эвтектику, можно по структуре определить содержание меди. Однако в этом случае надо учитывать количество меди, находящееся в эвтектике и в твердом растворе. Например, в доэвтектическом сплаве, содержащем 30 % эвтектики и 70 % твердого раствора, количество меди в эвтектике
 ,
,
а в твердом растворе
 .
.
Следовательно, исследуемый сплав содержит k x + k y = 14,06 % меди, что соответствует точке А, лежащей на оси абсцисс диаграммы состояния системы Al – CuAl 2 (рис. 1).
При определении
состава заэвтектических сплавов
рассчитывают количество меди, находящееся
в эвтектике и в химическом соединении
 .
Сумма этих количеств будет соответствовать
содержанию меди в заэвтектическом
сплаве. Химическое соединениеCuAl 2
отличается большой твердостью и
хрупкостью.
.
Сумма этих количеств будет соответствовать
содержанию меди в заэвтектическом
сплаве. Химическое соединениеCuAl 2
отличается большой твердостью и
хрупкостью.
В технике применяются преимущественно алюминиевые сплавы, содержащие 2…5 % меди, которые называются дуралюминами. Они хорошо обрабатываются давлением и имеют высокие механические свойства после термической обработки и нагартовки.
Дуралюмины применяют для изготовления деталей и элементов конструкций средней и повышенной прочности ( в = 420…520 МПа), требующих долговечности при переменных нагрузках, в строительных конструкциях.
Из дуралюмина изготовляют обшивки, шпангоуты, стрингеры и лонжероны самолетов, силовые каркасы и кузова грузовых автомобилей и т. д.

Сплавы Al с Si называют силуминами. Они обладают хорошими литейными свойствами и содержат 4…13 % Si. Из диаграммы состояния этих сплавов (рис. 3) следует, что силумины представляют собой доэвтектические или эвтектические сплавы, содержащие в структуре значительные количества эвтектики.
Однако при литье в обычных условиях эти сплавы приобретают неудовлетворительное строение, так как эвтектика получается грубопластинчатой, с крупными включениями хрупкого кремния, что сообщает сплавам низкие механические свойства.
На рис. 4, а представлена структура силумина марки АЛ2, содержащего 11…13 % Si. В соответствии с диаграммой состояния алюминий – кремний сплав такого состава имеет эвтектическое строение. Эвтектика состоит из -твердого раствора кремния в алюминии (светлый фон) и игольчатых крупных и хрупких кристаллов кремния. Игольчатые выделения частиц кремния создают внутренние острые надрезы в пластичном алюминии и приводят к преждевременному разрушению при нагружении.

Рис. 3. Диаграмма состояния системы Al–Si


Рис. 4. Силумин: а – до модифицирования, грубоигольчатая эвтектика (Al-Si) и первичные выделения кремния;б – после модифицирования, мелкодисперсная эвтектика
(Al-Si) и дендриты твердого раствора кремния и других элементов в алюминии
Введение модификатора меняет характер кристаллизации. Происходит смещение линий диаграммы состояния так, что сплав с 11…13 % кремния становится доэвтектическим.
В структуре появляются избыточные светлые зерна -твердого раствора (рис. 4, б ).
Модификатор изменяет форму частиц кремния: вместо игольчатых выпадают мелкие равноосные, не создающие опасных концентраций напряжений при нагружении.
В результате модифицирования предел прочности у данных сплавов повышается с 130 до 160 МПа, а относительное удлинение с 2 до 4 %.
В сплавах, обрабатываемых давлением, содержание кремния менее 1%. В алюминиевых сплавах, содержащих магний, кремний связывается с ним в устойчивое металлическое соединение Mg 2 Si; оно образует с алюминием диаграмму состояния эвтектического типа с ограниченными твердыми растворами (рис. 5).

Соединение Mg 2 Si отличается высокой твердостью, его переменная растворимость в алюминии позволяет достигать значительного упрочнения при термической обработке.
В электротехнике применяют алюминиевые сплавы типа альдрей, легированные магнием и кремнием. При старении закаленных сплавов Mg 2 Si выпадает из твердого раствора и упрочняет его. В результате такой обработки удается получит предел прочности до 350 МПа при относительном удлинении 10-15 %. Существенно, что электрическая проводимость такого сплава составляет 85 % электрической проводимости проводникового алюминия. Это обусловлено тем, что из твердого раствора при старении почти полностью удаляется Mg 2 Si и сплав состоит из чистого алюминия и упрочняющей фазы (Mg 2 Si).
Р ис.
6. Диаграмма состояния системыAl–Mg
ис.
6. Диаграмма состояния системыAl–Mg
Магний образует с алюминием твердые растворы, а также -фазу на основе соединения Mg 2 Al 3 . В большинство алюминиевых сплавов вводится магния не более 3 %, но в некоторых литейных сплавах типа магналия содержание его доходит до 12 %.
Как видно из рис. 6, в сплавах алюминия с магнием образуется эвтектика. Растворимость магния в алюминии сильно меняется с изменением температуры.
В качестве примера можно привести сплав АЛ8. В литом состоянии он имеет структуру, состоящую из зерен твердого раствора магния в алюминии и включений хрупкого соединения Al 3 Mg 2 .
После литья проводится гомогенизация при температуре 430 С в течение 15…20 часов, затем следует закалка в масле.
В процессе гомогенизации включения Al 3 Mg 2 полностью переходят в твердый раствор. Закаленный сплав приобретает достаточную прочность ( в = 300 МПа) и большую пластичность. Одновременно сплав приобретает высокую коррозионную стойкость. Старение для сплава АЛ8 является вредным: резко снижается пластичность и ухудшается коррозионная стойкость.
Цинк вводится в некоторые высокопрочные алюминиевые сплавы в количестве до 9 %. В двойных сплавах с алюминием при температуре выше 250 С цинк (в этих пределах) находится в твердом растворе (рис. 7).
 Рис.
7. Диаграмма состояния системыAl–Zn
Рис.
7. Диаграмма состояния системыAl–Zn
Все высокопрочные сплавы имеют сложный химический состав. Так, сплав В95 содержит 6 % Zn, 2,3 % Mg, 1,7 % Cu, 0,4 % Mn и 0,15 % Cr. Цинк, магний и медь образуют с алюминием твердые растворы и металлические соединения MgZn 2 , Al 2 CuMg – S-фаза, Mg 4 Zn 3 Al 3 – T-фаза. При нагревании эти металлические соединения растворяются в алюминии.
Например при температуре 475 ºС растворимость MgZn 2 в алюминии повышается до 18 % (рис. 8).
После закалки и искусственного старения сплав В95 имеет в = 600 МПа, = 12 %. Марганец и хром усиливают эффект старения и повышают коррозионную стойкость сплава.

(мас.)
Рис. 8. Диаграмма состояния системы Al–MgZn 2
Правила техники безопасности
1. Соблюдать все меры предосторожности и правила техники безопасности при приготовлении микрошлифов.
2. При шлифовании микрошлифа следует чаще охлаждать образец, чтобы не допускать ожогов пальцев рук.
3. При травлении шлифов пользоваться резиновыми перчатками.
4. При изучении структуры сплава на микроскопе следует убедиться, что он надежно заземлен.
5. Следует пользовать только исправным инструментом и оснасткой.
Порядок выполнения работы
1. Изучить диаграмму состояний алюминиевых сплавов.
2. Дать характеристику заданного сплава (структуру, фазовые превращения, состав, свойства, область применения).
3. Зарисовать структуру исследуемого сплава.
Зарисовки микроструктур изученных сплавов с указанием фаз и структурных составляющих.
Копирование диаграммы фазового равновесия, указанной преподавателем.
Для сплава заданного состава описание всех фазовых превращений при нагреве или охлаждении и определение химического состава фаз.
Контрольные вопросы
Почему коррозионная стойкость многих алюминиевых сплавов ниже коррозионной стойкости чистого алюминия?
Можно ли по микроструктуре сплава определить тип сплава – литейный или деформируемый?
Какова структура деформируемых алюминиевых сплавов, не упрочняемых термической обработкой?
Каким путем достигается упрочнение однофазных алюминиевых сплавов?
Какова упрочняющая термическая обработка двухфазных алюминиевых сплавов?
Что является целью закалки дуралюмина?
Каковы основные механические свойства дуралюмина?
Какие сплавы называются силуминами?
Какова удельная прочность алюминиевых сплавов?
Основные легирующие элементы в алюминиевых сплавах.
Анализ полученных результатов выбора легирующих элементов для алюминия показывает, что наибольшее упрочнение обеспечивает магний, так как для него характерно наличие двух механизмов упрочнения – твердо-растворный – за счет критерия α (18,9) и с помощью термообработки γ = 0,57. Более высокой технологической пластичностью и жаропрочностью обладают сплавы системы Al-Mn, так как критерии ω и τ для них имеют наибольшее значение. – 0,77 и 0,99, соответственно. Кроме того, в них слабее всего развита пористость, поскольку величина критерия δ минимальна. Однако они не подвергаются упрочняющей термообработке как алюминиево-магниевые сплавы: для них γ = 0,96 вместо 0,57.
Максимальной жидкотекучестью, в соответствии с определением критерия λ, обладают сплавы системы Al-Si, его значение наиболее высокое из рассмотренных легирующих добавок – 7,3 вместо 6,5 у меди и 5,3 – у магния. Силумины обладают достаточно высокой жаропрочностью – τ=0,91, что лишь немногим меньше, чем у марганца. Их существенным недостатком является низкая технологическая пластичность, ω=0,13, вместо 0,77- у марганца и 0,50 – у магния и невозможность термического упрочнения – γ=0,98.
Обобщая вышеизложенное, можно констатировать, что основными деформируемыми сплавами, не подвергающимися термической обработке, являются сплавы системы Al-Mn, термически упрочняемыми - Al-Mg, литейными - Al-Si. Эти результаты хорошо известны, и их ценность заключается в том, что предложенные Б.Б. Гуляевым критерии диаграмм состояния отражают истинное положение вещей и могут быть использованы при выборе легирующих элементов для формирования заданного уровня эксплуатационных и технологических свойств для всех без исключения основ сплавов.
4.4.5 Диаграммы состояния двойных сплавов алюминия
В качестве примера для освоения методики выбора легирующих элементов и комплексов сплавов на основе алюминия использованы наиболее известные, сведения о которых широко изложены в технической и справочной литературе .
| Рисунок 4.4. Диаграмма состояния Al-Ga |
 | |
| Рисунок 4.5. Диаграмма состояния Al-Ge | |
 | |
| Рисунок 4.6. Диаграмма состояния Al-Li |
 | |
| Рисунок 4.7. Диаграмма состояния Al-Ag | |
 | |
| Рисунок 4.8. Диаграмма состояния Al-Cu | |
 | |
| Рисунок 4.9. Диаграмма состояния Al-Zn | |
 | |
| Рисунок 4.10. Диаграмма состояния Al-Mg | |
 | |
| Рисунок 4.11. Диаграмма состояния Al-Mn | |
 | |
| Рисунок 4.12. Диаграмма состояния Al-Si |